经国家食品药品监督管理局批准(批件号:2014L00508 ),长春金赛药业股份有限公司将在华中科技大学同济医学院附属同济医院、湖南省儿童医院、首都儿研所、吉林大学第一医院、无锡市第四人民医院、复旦儿科医院、上海新华医院、江西省儿童医院对已上市长效生长激素(商品名:“金赛增”),进行扩大适应症的临床研究,现需要招募多名符合条件的患儿进行免费治疗,要求基本条件如下:
⑴ 临床诊断为足月小于胎龄儿患者;
⑵ 女孩 3-6 周岁、男孩 3-7 周岁;
⑶ 青春期前(TannerI期);
⑷ 入组时没有实现追赶生长 (追赶生长定义为身高达到同年龄、同性别儿童身高的第 3
百分数以上);
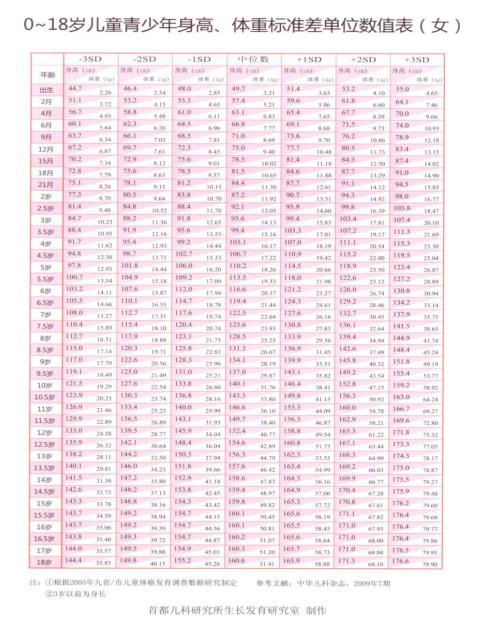
⑸ 入组时身高低于同年龄同性别正常儿童中位数的-2SDS;
⑹ 入组前一年内任一项生长激素激发试验之后,血清生长激素的峰浓度>10g/L;
⑺ 骨龄≤实际年龄+1;
⑻ 糖调节功能正常:空腹血糖 < 5.6mmol/L;
⑼ 出生胎龄 ≥ 37 周;
⑽ 受试者及其监护人均签署知情同意书 。
受益:受试患儿参加临床研究期间所应用的研究用药物及相关的检查都是免费的。在 1 年的临床试验治疗结束后,如果受试患儿及其监护人同意,患儿将继续免费获得适宜剂量的长效生长激素进行治疗,直至患儿达到成年终身高
符合以上条件的患儿,我们将统一安排时间进行初筛,热诚欢迎广大有需求的矮小患儿参与!
联系电话:手机:400-820-0469 座机:800-820-0469
附录1 中国15城市不同胎龄男、女新生儿出生体重百分比位数修正值

附录4 中国9城市 0-18岁儿童身高、体重标准差单位数值表(2005年,男性)

附录5中国9城市 0-18岁儿童身高、体重标准差单位数值表(2005年,女性)